Sie haben kein Konto?

NANOCOLL
0,5 mg, Kit für ein radioaktives Arzneimittel/Pulver zur Herstellung einer Injektionssuspension
Zusammensetzung:
Eine Durchstechflasche enthält: 0,5 mg Albumin vom Menschen, denaturiert; 0,2 mg Zinn(II)-chlorid-Dihydrat; D-Glucose; Poloxamer 238; Dinatriumhydrogenphosphat; Dodecanatriumfitat.
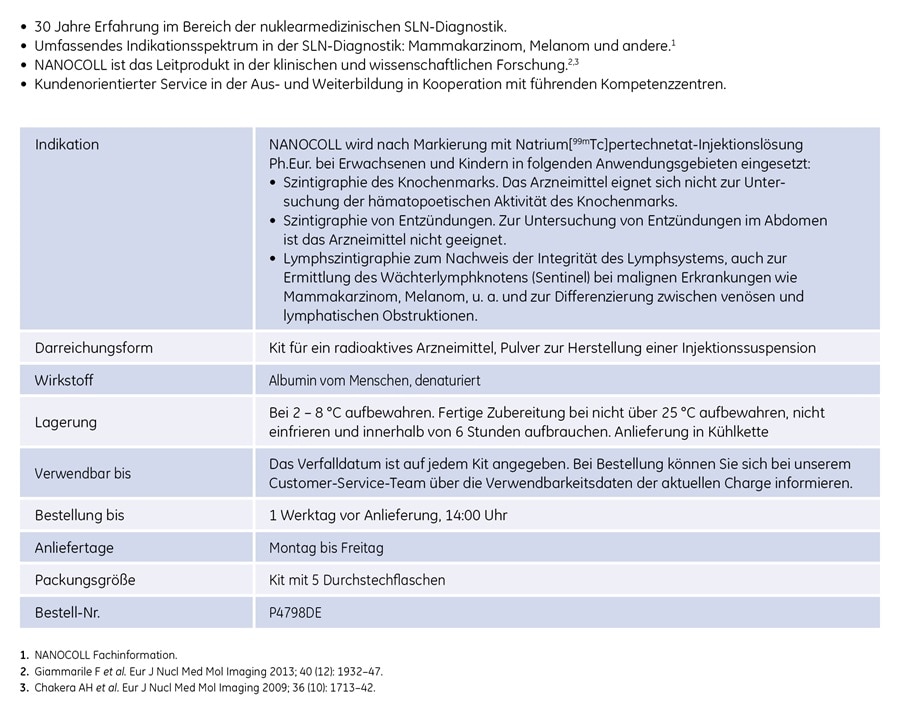
Anwendungsgebiete:
Dieses Arzneimittel ist nur für diagnostische Zwecke bestimmt.
NANOCOLL wird nach Markierung mit Natrium[99mTc]pertechnetat-Injektionslösung Ph.Eur. bei Erwachsenen und Kindern in folgenden
Anwendungsgebieten eingesetzt:
Gegenanzeigen:
Anwendungseinschränkungen:
Bei jedem Patienten ist sorgfältig zwischen dem zu erwartenden diagnostischen Nutzen und dem mit der Strahlenexposition verbundenen Risiko abzuwägen. Um die diagnostische Information zu erhalten, darf die anzuwendende Aktivität nicht höher als erforderlich bemessen werden.
Bei Patienten mit Nieren- oder Leberfunktionsstörung ist eine sorgfältige Abwägung des Nutzen/Risiko-Verhältnisses erforderlich, da es zu einer erhöhten Strahlenbelastung kommen kann.
Bei Kindern und Jugendlichen ist eine sorgfältige Prüfung der Indikation notwendig, da die effektive Dosis pro MBq höher ist als bei Erwachsenen.
Patienten sollen vor der Untersuchung ausreichend trinken. Um die Strahlenexposition zu reduzieren, müssen die Patienten aufgefordert werden, während der ersten Stunden nach der Untersuchung so oft wie möglich die Blase zu entleeren.
Bei Patienten mit völliger Lymphobstruktion ist eine Lymphszintigraphie wegen der Gefahr des Entstehens von Strahlennekrosen an der Injektionsstelle nicht ratsam.
NANOCOLL enthält Natrium, aber weniger als 1 mmol (23 mg) Natrium pro Durchstechflasche, d. h. es ist nahezu „natriumfrei“.
Die Möglichkeit von Überempfindlichkeitsreaktionen, einschließlich schwerwiegender, lebensbedrohlicher oder tödlicher anaphylaktischer oder anaphylaktoider Reaktionen muss stets in Betracht gezogen werden.
Bei Auftreten von Überempfindlichkeitsreaktionen, einschließlich anaphylaktischer Reaktionen, darf keine weitere Zufuhr des Arzneimittels erfolgen. Falls notwendig, sind entsprechende Gegenmaßnahmen einzuleiten. Um im Notfall unverzüglich reagieren zu können, sollten entsprechende Instrumente (u. a. Trachealtubus und Beatmungsgerät) und Medikamente griffbereit sein.
Das in NANOCOLL enthaltene Humanalbumin entspricht den Anforderungen der "Note for Guidance on Plasma Derived Products", CPMP/BWP/269/95, rev. 2. Dennoch kann das Risiko einer Übertragung infektiöser Krankheitserreger bei einer Verabreichung von Arzneimitteln, die Blutbestandteile enthalten, nicht mit endgültiger Sicherheit ausgeschlossen werden. Dies gilt auch für Krankheitserreger, deren Natur heute noch unbekannt ist. Bei der Anwendung von NANOCOLL wird empfohlen die jeweilige Chargenbezeichnung in der Patientendokumentation festzuhalten.
Frauen im gebärfähigen Alter: Falls es erforderlich ist, an einer Frau im gebärfähigen Alter ein radioaktives Arzneimittel anzuwenden, ist festzustellen, ob eine Schwangerschaft vorliegt. Grundsätzlich muss von einer Schwangerschaft ausgegangen werden, wenn eine Menstruation ausgeblieben ist. Im Zweifelsfall einer potentiellen Schwangerschaft (wenn eine Menstruation ausgeblieben ist, die Periode sehr unregelmäßig ist, etc.) sollten der Patientin alternative Untersuchungsmethoden ohne ionisierende Strahlung (falls vorhanden) angeboten werden.
Subkutane Anwendung während der Schwangerschaft: Während der Schwangerschaft ist die subkutane Anwendung von 99mTc-Albumin-Nanokolloid für die Lymphszintigraphie aufgrund der möglichen Konzentration in den Pelvislymphknoten strengstens kontraindiziert. Im Zweifelsfalle ist ein Schwangerschaftstest durchzuführen.
Intravenöse Anwendung während der Schwangerschaft: Nuklearmedizinische Untersuchungen bei Schwangeren beinhalten auch eine Strahlenexposition des Feten. Daher sollten während der Schwangerschaft nur absolut unerlässliche Untersuchungen durchgeführt werden, bei denen der zu erwartende Nutzen das Risiko für Mutter und Kind bei Weitem übersteigt. Die intravenöse Verabreichung von 500 MBq 99mTc-Albumin-Nanokolloid ergibt eine im Uterus absorbierte Dosis von 0,9 mGy. Strahlendosen über 0,5 mGy werden als potentielles Risiko für den Feten betrachtet.
Stillzeit: Vor Anwendung eines radioaktiven Arzneimittels an einer stillenden Mutter ist zu prüfen, ob die Untersuchung nicht auf einen Zeitpunkt nach dem Abstillen verschoben werden kann und welches Radiopharmazeutikum im Hinblick auf die Aktivitätsausscheidung in die Muttermilch am besten geeignet ist. Falls eine Anwendung während der Stillzeit unumgänglich ist, muss das Stillen bis mindestens 13 Stunden nach Injektion unterbrochen und die abgepumpte Muttermilch verworfen werden.
Nebenwirkungen:
Erkrankung des Immunsystems:
Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar: Überempfindlichkeit, Anaphylaxie
Ionisierende Strahlen können Krebs und Erbgutveränderungen verursachen. Da die effektive Strahlendosis bei Gabe der maximalen empfohlenen Aktivität von 500 MBq bei 2,5 mSv liegt, sind diese Nebenwirkungen mit geringer Wahrscheinlichkeit zu erwarten.
Verschreibungspflichtig.
Stand der Information: März 2015
GE Healthcare Buchler GmbH & Co. KG
Gieselweg 1, 38110 Braunschweig